Un système implantaire novateur au service de l'implantologie minimalement invasive
Présentation d'un système alliant chirurgie guidée et implant économe en tissus.
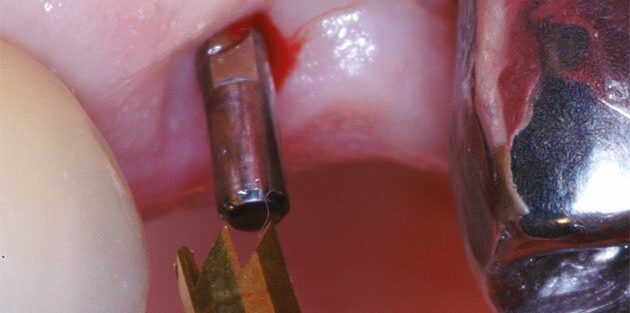
Le processus d'ostéointégration des implants dentaires décrit depuis maintenant plus de 40 ans [1] a permis d'offrir aux patients édentés des traitements alternatifs aux bridges et appareils amovibles.
Depuis cette découverte, les challenges successifs ont été de proposer aux patients des protocoles de plus en plus sûrs et prédictibles, aussi bien pour la cicatrisation des tissus péri-implantaires que pour les restaurations prothétiques [1][2].
En 1969 déjà, les auteurs rapportaient les incidences délétères de l'exposition osseuse lors de la chirurgie, sur la cicatrisation [3][4][5]. Dans les années 2000, les premières publications sur la chirurgie minimalement invasive en implantologie - (chirurgie sans lambeau, dite...
Ce contenu est réservé aux utilisateurs inscrits sur le site dentaire365.fr
Déjà abonné ? Connectez-vous